Malattie
rare, il calvario delle famiglie
Malattie rare: ancora nel 2011 queste parole si trovano ad
essere in qualche modo sinonimo di calvario. Per le famiglie, per le persone
malate. Non si tratta solo del problema prettamente fisico di affrontare
una
patologia
quasi sconosciuta, ma anche di quello organizzativo relativo all’ avere a che
fare con una burocrazia lenta e non aggiornata.
E spesso solo la rete rappresenta un alleato. Perché i problemi sono molti,
la conoscenza poca, e per trovare del
sostegno specializzato
od ottenere semplicemente una
diagnosi, non di rado passano
anni.
Vi sono malattie rare tipo la
Sindrome di Kabuki, che solo
recentemente hanno trovato il giusto sostegno a livello medico. Ma gli
specialisti in tal senso sono pochi. E per ottenere delle
cure
appropriate, bisogna spostarsi, con il conseguente carico economico e di
stress.
Specialmente se si tratta di bambini. Perché quando si parla di particolari
sindromi,
sono proprio loro le piccole vittime. Ed immaginate un bambino di qualche mese
o di pochi anni sottoposto a veri e propri viaggi della speranza corredati da
un continuo avvicendarsi di
esami specialistici, risonanze
magnetiche.
Uno stress inappropriato, ma necessario. Al quale ovviamente, scoperta la
malattia,
si aggiunge l’ignoranza della gente. Perché spesso e volentieri i malati di
malattie rare sono sottoposti ad un trattamento quasi “razzista”. Squadrati
dalla testa ai piedi, quasi in ogni occasione, alla
sofferenza fisica
debbono aggiungere quella psicologica derivante non solo dall’essere dipendenti
da
terapie di ogni sorta, ma anche dall’allontanamento, più o
meno volontario, da parte dei coetanei.
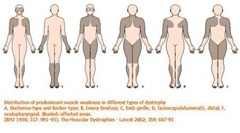
E se una malattia come la
mucopolisaccaridosi, di gravità
variabile a seconda della tipologia, porta quasi sempre all’indossare un busto
per tentare di mantenere un corretto sviluppo dello scheletro, vi sono tante
patologie per le quali, il sistema sanitario nazionale, pur
riconoscendole invalidanti, non passa i
farmaci.
Ciò che la maggior parte della famiglie lamentano è però la lentezza
della burocrazia, ed in qualche modo la sua ignoranza. Essere affetti da una
malattia rara nella maggior parte dei casi significa combattere continuamente
con gli uffici preposti sul territorio per il riconoscimento dell’
invalidità
e tutte le pratiche assistenziali ad essa correlata.
firma